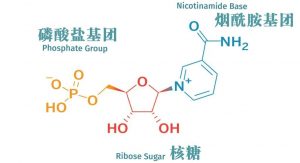
NMN代表烟酰胺单核苷酸,是一种自然存在于所有生命形式中的分子。在分子水平上,该分子是核糖核苷酸,是核酸RNA的基本结构单位。在结构上,它由烟酰胺基团、核糖和磷酸盐基团组成(上图)。NMN是人体必需分子烟酰胺腺嘌呤二核苷酸(NAD+)的直接前体,被认为是提高细胞NAD+水平的关键分子。什么是烟酰胺腺嘌呤二核苷酸(NAD+)?
NAD+是生命和细胞功能所必需的必需辅酶。酶是生化反应催化剂,没有酶,就没有生命。辅酶是酶功能所需的“辅助”分子。NAD+能做什么?
NAD+是身体中除了水之外最丰富的分子,没有它,有机体就会死亡。NAD+被人体内的许多蛋白质所使用,例如修复受损DNA的sirtuins。对线粒体也很重要,线粒体是细胞的动力源,产生我们身体所使用的化学能量。
NAD+在代谢过程中起着特别积极的作用,如糖酵解、TCA循环(AKA、Krebs循环或柠檬酸循环)和电子传递链,它们发生在我们的线粒体中,是获得细胞能量的必经过程。作为配体,NAD+与酶结合并在分子间传递电子。
电子是细胞能量的原子基础,通过将它们从一个分子转移到下一个分子,NAD+通过类似于充电电池的细胞机制起作用。当电子被消耗以提供能量时,电池就会耗尽。这些电子不能在没有提升的情况下回到它们的起点。在细胞中,NAD+起着促进作用。这样,NAD+可以降低或增加酶活性、基因表达和细胞信号。
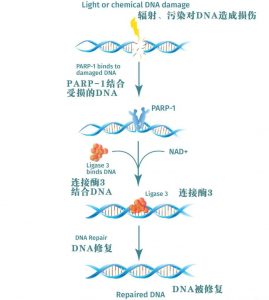
随着生物体年龄的增长,由于辐射、污染和DNA复制不精确等环境因素,它们会产生DNA损伤。根据目前的衰老理论,DNA损伤的积累是衰老的主要原因。几乎所有的细胞都含有修复这种损伤的“分子机制。这种机器消耗NAD+和能量分子。
因此,过量的DNA损伤会耗尽宝贵的细胞资源。一种重要的DNA修复蛋白,PARP(Poly(ADP-核糖)聚合酶),依赖于NAD+功能,NAD+能够修复受损DNA(点击查看文章)。
老年人的NAD+水平降低。正常老化过程导致DNA损伤的积累导致PARP增加,从而导致NAD+浓度降低。线粒体中任何进一步的DNA损伤都会加剧这种耗竭。

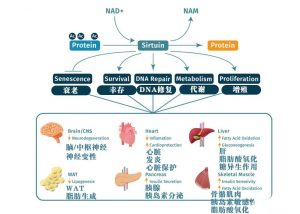
NAD+影响sirtuins(长寿基因)的活动新发现的sirtuins,也被称为“基因的守护者”,在维持细胞健康方面起着至关重要的作用。sirtuins是一个酶系,参与细胞应激反应和损伤修复。他们还参与胰岛素分泌、衰老过程和衰老相关的健康状况,如神经退行性疾病和糖尿病。激活sirtuins需要NAD+。
正如哈佛遗传学家和NAD研究人员大卫·辛克莱(David Sinclair)所说,随着年龄的增长,我们失去了NAD+,并因此导致sirtuin活性的下降,这被认为是导致老年病的主要因素。为什么我们要关心NAD+?
自从1906年发现NAD+以来,该分子一直在科学家的关注焦点中,因为它大量存在于人体细胞以及它在维持我们身体运行的分子途径中的关键作用。在动物研究中,提高体内NAD+水平在代谢和年龄相关疾病等研究领域显示出了有希望的结果,显示了一些抗衰老特性,并作用于与年龄有关的疾病,如糖尿病、心血管疾病、神经变性和免疫系统衰弱。
衰老
NAD+是帮助sirtuins维持基因组完整性和促进DNA修复的燃料。就像汽车开动不能没有燃料一样,sirtuins的激活需要NAD+。动物研究结果表明,提高体内NAD+水平可激活sirtuins,增加酵母、蠕虫和小鼠的寿命。动物研究在抗衰老特性方面显示出有希望的结果,科学家们正研究如何将此更好作用于人类。
代谢紊乱NAD+是维持健康线粒体功能和稳定能量输出的关键之一。衰老和高脂饮食可降低体内NAD+水平。小鼠研究表明,服用NAD+补充剂可以减轻因为饮食和衰老导致的体重增加,并提高他们的运动能力。
其他研究甚至改变了雌性小鼠的糖尿病效应,显示了对抗代谢性疾病(例如肥胖症)的新策略。心脏功能提高NAD+水平可以保护心脏,改善心脏功能。高血压会导致心脏增大,动脉阻塞,导致中风。在小鼠实验中,NAD+助推器补充了心脏的NAD+水平,并防止了由于缺乏血流而对心脏造成的伤害。其他研究表明,NAD+补充剂可以保护小鼠免受异常心脏增大的影响。
在阿尔茨海默病小鼠中,提高其NAD+水平会降低蛋白质的积累,从而破坏大脑中的细胞交流,从而增加认知功能。提高NAD+水平也能保护脑细胞在血液流向大脑不足时不会死亡。在动物模型中的许多研究提出了新的前景,以帮助大脑健康的年龄,防御神经变性和改善记忆。
随着人年龄的不断增长,免疫系统下降,人们更容易生病,也更难从季节性流感等疾病中恢复过来。最近的研究表明,NAD+水平在调节免疫反应和衰老过程中的炎症和细胞存活中起着重要作用。该研究强调了NAD+对免疫功能障碍的治疗潜力。身体如何制造烟酰胺腺嘌呤二核苷酸(NAD+)?
我们的身体能自然地产生NAD+。体内产生NAD+的前体主要有五种:色氨酸,烟酰胺(Nam),烟酸(NA),烟酰胺核苷(NR),烟酰胺单核苷酸(NMN)。其中,NMN代表NAD+合成的最后步骤之一,这些NAD+的产生都可以来自饮食。纳米、NA和NR都是维生素B3的一种重要营养物质。一旦进入体内,我们的细胞就可以通过几种不同的途径合成NAD+。
这种生化反应途径相当于工厂生产线,多条生产线都生产相同的产品。除了从NAD+前体色氨酸产生NAD+外,还有另一种方式:称为补救途径。补救途径类似于回收,因为它从NAD+降解的产物中产生NAD+。身体内的所有蛋白质都需要定期降解,以阻止它们积累到不健康的程度。作为这一生产和降解周期的一部分,酶将蛋白质降解后放回同一蛋白质的生产线中。
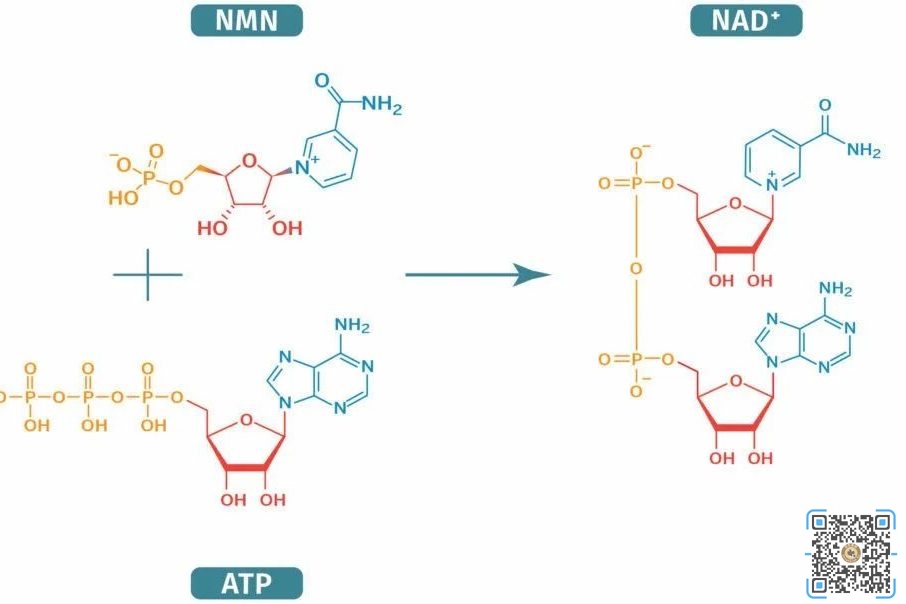
身体中NMN是如何合成的?NMN是由体内的B族维生素产生的。负责在体内制造NMN的酶称为烟酰胺磷酰基转移酶(NAPT)。NAPT将烟酰胺(一种维生素B3)附着在一种称为PRPP(5‘-磷酰-1-焦磷酸)的糖磷酸盐上)。NMN也可以通过添加磷酸盐基团由“烟酰胺核苷”(NR)制成。“NAMPT”是NAD+生产中的限速酶。这意味着低水平的NAMPT导致NMN产量下降,导致NAD+水平下降。添加像NMN这样的前体分子可以加快NAD的+生成。
禁食或减少热量摄入,又称控制热量,已被证明可以增加NAD+水平和sirtuin活性。在小鼠实验中,来自热量限制的NAD+和sirtuin活性的增加已经被证明可以减缓衰老过程。虽然NAD+存在于一些食物中,但浓度太低,不能影响细胞内浓度。服用某些补充剂,如NMN,已被证明会增加NAD+水平。作为NAD+补充的NMN
细胞内NAD+浓度会随着正常细胞功能的消耗、时间的推移而减少。
健康的NAD+水平被认为是可以通过补充NAD+前体来恢复的。根据研究,NMN和烟酰胺核苷(NR)等前体被认为是NAD+生产的补充,能够增加NAD+的浓度。哈佛大学的NAD+研究员大卫辛克莱说,“直接给生物体喂食或提供NAD+不是一个实际的选择。NAD+分子不能很容易地穿过细胞膜进入细胞,因此将无法积极影响代谢。相反,必须使用NAD+的前体分子来提高NAD+的生物有效性水平。“这意味着NAD+不能用作直接补充,因为它不容易被吸收。NAD+前体比NAD+更容易被吸收,是更有效的补充剂。
NMN补充如何吸收和作用于整个身体?
NMN通过嵌入在细胞表面的分子转运体被吸收到细胞中。与NAD+相比,NMN分子可以更有效地吸收到细胞中。因为细胞膜这道屏障,NAD+不能轻易进入人体。膜有一个无水的空间,可以防止离子、活性分子和大分子在无转运体的情况下进入。
人们曾经认为NMN在进入细胞之前会发生改变,但新的证据表明,它可以通过细胞膜上的NMN特异性转运体直接进入细胞。此外,注射NMN会快速扩大体内的NAD+分布区区域,包括胰腺、脂肪组织、心脏、骨骼肌、肾脏、睾丸、眼睛和血管。在小鼠实验中口服NMN可在15分钟内增加肝脏中的NAD+。
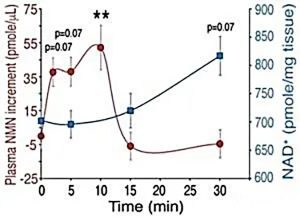
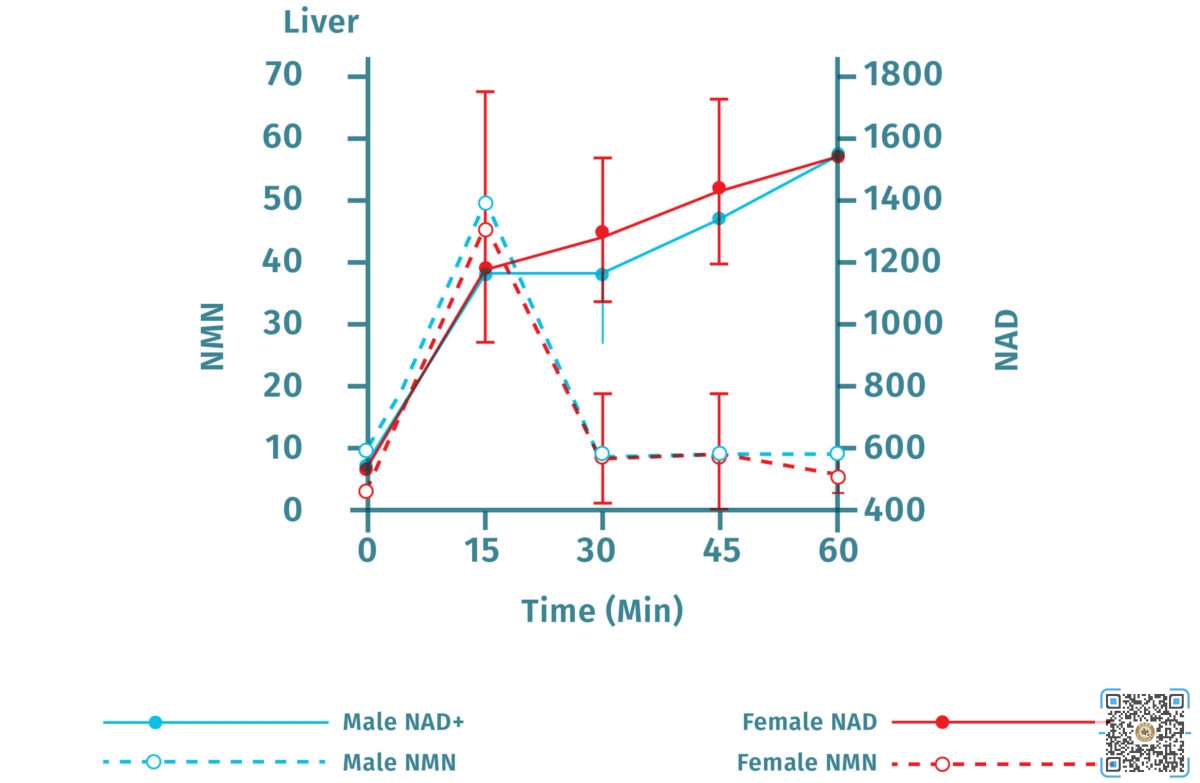
NMN在动物实验中被认为是安全的,结果是有希望的。这种分子在很大程度上被认为是安全的,而不是有毒的,即使在小鼠和人类的实验中浓度很高。小鼠长期(一年)口服不具有毒性作用。人类的第一个临床试验已经完成,证据支持了一种观点,即它在单一剂量下是无毒的。虽然2019年11月发表的一项对日本男性的研究指出,NMN给药后,受试者血液中胆红素水平升高,但这些水平仍在正常范围内。未来的研究应该集中在使用的长期安全性和有效性上。NMN与任何其他已知的副作用无关。
烟酰胺腺嘌呤二核苷酸,简称NAD,是人体最重要、最通用的分子之一。因为它是为细胞提供能量的核心,所以几乎没有不需要NAD的生物过程。因此,NAD是广泛生物研究的重点。1906年,亚瑟·哈登和威廉·约翰·杨在从啤酒酵母中提取的液体中发现了一个“因子”,它促进了糖向酒精的发酵。那个“因子”,当时被称为“协助因子”,结果是NAD。哈登和汉斯·冯·欧拉-谢尔平继续揭开发酵的奥秘。
他们获得了1929年的诺贝尔奖,因为他们对这些过程有了详细的了解,包括不久将被称为NAD的化学形状和性质。20世纪30年代,在另一位诺贝尔奖得主奥托·沃伯格(Otto Warburg)的指导下,NAD在促进许多生化反应方面发挥了核心作用。Warburg发现NAD作为电子的生物继电器:电子从一个分子转移到另一个分子,作为执行所有生化反应所需的能量的基础。
1937年,麦迪逊威斯康星大学的Conrad Elvehjem和他的同事发现,NAD+补充治愈了狗的“ Otto Warburg”病又称“黑舌”病。在人类中,Otto Warburg会引起许多症状,包括腹泻、痴呆和口腔溃疡。它起源于烟酸缺乏,现在定期用烟酰胺治疗,烟酰胺是NMN的前体之一。
亚瑟·科恩伯格在40和50年代对NAD+的研究有助于他发现DNA复制和RNA转录背后的原理,这两个过程对生命至关重要。1958年,Jack Preiss和Philip Handler发现了三个生化步骤,烟酸被转化为NAD。
这一系列的步骤,称为路径,今天被称为Preiss-Handler路径。1963年,Chambon、Weill和Mandel报告说,烟酰胺单核苷酸(NMN)提供了激活一种重要核酶所需的能量。这一发现为一种叫做PARP的蛋白质的一系列显著发现铺平了道路。PARPs在修复DNA损伤、调节细胞死亡方面起着至关重要的作用,其活性与寿命的变化有关。在1976年,Rechsteiner和他的同事发现了令人信服的证据,NAD+似乎可能在哺乳动物细胞中具有“其他主要功能”,超出了其作为能量转移分子的经典生化作用。这一发现使Leonard Guarente和他的同事有可能发现,sirtuins蛋白质通过不同的保持某些基因“沉默”来延长寿命。”自那时以来,人们对NAD及其中间产物NMN和NR越来越感兴趣,因为它们有可能改善一些与年龄有关的健康问题。
NMN的未来
随着NMN在动物研究中显示出的有前途的治疗特性,研究人员正在试图了解这种分子是如何在人体中工作的。日本最近的一项临床试验表明,该分子在使用剂量下是安全和耐受性好的。更多的研究和人类试验正在进行中。它是一个令人着迷的、作用良多的分子,我们仍然有很多东西要学。
这么多理论,我该记住些什么?
1、NAD+参与了身体每个生理进程,而这种重要的物质会随着年龄增长而减少。
2、NMN是一种NAD+补充剂,比直接补充NAD还能更好地可以补充和恢复人体NAD+水平。
3、NMN已被证实是有效、安全的NAD+补充剂。
https://www.nmn.com/precursors/what-is-nmn
翻译:Calerie
参考文献(Journal Reference):
Vincenzo Carafa, Dante Rotili, Mariantonietta Forgione,
Francesca Cuomo, Enrica Serretiello, Gebremedhin Solomon Hailu, Elina Jarho, Maija Lahtela-Kakkonen, Antonello Mai, Lucia Altucci. Sirtuin functions and modulation: from chemistry to the clinic. Clin epigenetics, 2016;
DOI: 10.1186/s13148-016-0224-3.
Niels J. Connell, Riekelt H. Houtkooper, Patrick Schrauwen. NAD+ metabolism as a target for metabolic health: have we found the silver bullet? Diabetologia, 2019; DOI: 10.1007/s00125-019-4831-3.
Julia Evangelou. “Natural compound reduces signs of aging in healthy mice.” ScienceDaily.com. 27 October 2016. Web. 16 January. 2020.
Henryk Jęśko, Przemysław Wencel, Robert P. Strosznajder, Joanna B. Strosznajder. Sirtuins and Their Roles in Brain Aging and Neurodegenerative Disorders. Neurochem Res, 2017; DOI: 10.1007/s11064-016-2110-y.
Ann Katrin-Hopp, Patrick Grüter, Michael O. Hottiger. Regulation of Glucose Metabolism by NAD+ and ADP-Ribosylation. Cells, 2019;
DOI: 10.3390/cells8080890.
Vamshi K.C. Nimmagadda, Tapas K. Makar, Krish Chandrasekaran, Avinash Rao Sagi, Jayanta Ray, James W. Russell, Christopher T Bever Jr. SIRT1 and NAD+ precursors: Therapeutic targets in multiple sclerosis a review. J Neuroimmunol, 2017; DOI: 10.1016/j.jneuroim.2016.07.007.
Katalin Sas, Elza Szabó, László Vécsei. Mitochondria, Oxidative Stress and the Kynurenine System, with a Focus on Ageing and Neuroprotection. Molecules, 2018; DOI: 10.3390/molecules23010191.
Yue Yang, Anthony A. Sauve. NAD+ metabolism: Bioenergetics, signaling, and manipulation for therapy. Biochim Biophys Acta, 2016; DOI: 10.1016/j.bbapap.2016.06.014.
Jun Yoshino, Kathryn F. Mills, Myeong Jin Yoon, Shin-ichiro Imai. Nicotinamide Mononucleotide, a Key NAD+ Intermediate,
Treats the Pathophysiology of Diet- and Age-Induced Diabetes in Mice. Cell Metab, 2011; DOI: 10.1016/j.cmet.2011.08.014.
Mills KF, Yoshida S, Stein LR, Grozio A, Kubota S, Sasaki Y, Redpath P, Migaud ME, Apte RS, Uchida K, Yoshino J, Imai SI. Long-Term Administration of Nicotinamide Mononucleotide Mitigates Age-Associated Physiological Decline in Mice. Cell Metab, 2016; DOI: 10.1016/j.cmet.2016.09.013.
Shuang Zhou, Xiaoqiang Tang, Hou-Zao Chen. Sirtuins and Insulin Resistance. Front Endocrinol (Lausanne), 2018; DOI: 10.3389/fendo.2018.00748.
Irie J, Inagaki E, Fujita M, et al. Effect of oral administration of nicotinamide mononucleotide on clinical parameters and nicotinamide metabolite levels in healthy Japanese men, 2019 Nov 2]. Endocr J. 2019;
10.1507/endocrj.EJ19-0313. doi:10.1507/endocrj.EJ19-0313关于NMN.com
4,139 total views, 5 views today

